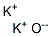
CAS号:12136-45-7
|
英文名称:Potassium oxide
分子式
K2O
分子量
94
EINECS号
235-227-6
MDL
Smiles
InChIKey
氧化钾化学百科
基本信息
| 中文名称 | 氧化钾 |
| 英文名称 | Potassium oxide |
| CAS号 | 12136-45-7 |
| 分子式 | K2O |
| 分子量 | 94.196 |
| EINECS号 | 235-227-6 |
物化性质
| 熔点 | decomposes at 350℃ [HAW93] |
| 沸点 | 691.46℃[at 101 325 Pa] |
| 密度 | 2.350 |
| 蒸气压 | 0Pa at 25℃ |
| LogP | -5.08 at 25℃ |
| 溶解度 | 溶于水、乙醇、乙醚 |
| 形态 | 灰色立方晶体 |
| 颜色 | 灰色立方晶体、结晶 |
| 水溶解性 | soluble H2O, forming KOH; soluble alcohol and ether [HAW93] |
| 晶体结构 | Reverse CaF2 type |
安全信息
| 危险品运输编号 | 2033 |
| 危险等级 | 8 |
| 包装类别 | II |
生产及用途
氧化钾为碱金属氧化物,在自然界不单独存在。陶瓷工业上,多用长石引入,作用与氧化钠相似。
氧化钾主要用于无机工业,是制造各种钾盐如氢氧化钾、硫酸钾、硝酸钾、氯酸钾、红矾钾等的基本原料。
生产方法
用金属钾控制氧化可制取氧化钾。
首先,要除去金属钾表面的难挥发的油类物质,为此须将金属钾在二甲苯中反复熔融数次,然后置于硬质玻璃管中用泵抽气蒸馏二次,以排除其中的气体,经这样处理的金属钾的表面是光洁的。将其在高真空中通过一支毛细管滤入一个高硅玻璃制的器皿中,将其微微加热,并以很小的量通入干燥的纯空气,通入数次则生成微粒状的氧化钾。尚未反应的金属钾由于反应热而熔融,被吸附在海绵状的氧化钾表面,形成具有金属光泽的聚集体,这样可以避免生成过氧化钾。最后,将过量的金属钾在350℃真空蒸馏除去,器皿中剩余的氧化钾纯度可达99.5%。
上下游产品
上游产品共计:0个
下游产品共计:0个
相关产品
-
CAS号:10097-28-6
一氧化硅 -
CAS号:1310-58-3
氢氧化钾 , 85+% -
CAS号:298-14-6
碳酸氢钾 -
CAS号:24572-01-8
氘氧化钾 溶液 -
CAS号:7758-94-3
氯化亚铁 -
CAS号:20427-58-1
氢氧化锌 -
CAS号:12125-03-0
锡酸钾 三水合物 -
CAS号:3917-15-5
烯丙基乙烯基醚 -
CAS号:1309-48-4
氧化镁 , 用于分析 -
CAS号:1314-56-3
五氧化二磷 -
CAS号:7778-80-5
硫酸钾 -
CAS号:10097-28-6
一氧化硅 -
CAS号:1310-58-3
氢氧化钾 , 85+% -
CAS号:298-14-6
碳酸氢钾 -
CAS号:24572-01-8
氘氧化钾 溶液 -
CAS号:7758-94-3
氯化亚铁 -
CAS号:20427-58-1
氢氧化锌 -
CAS号:12125-03-0
锡酸钾 三水合物 -
CAS号:3917-15-5
烯丙基乙烯基醚 -
CAS号:1309-48-4
氧化镁 , 用于分析 -
CAS号:1314-56-3
五氧化二磷 -
CAS号:7778-80-5
硫酸钾
产品供应商

