| 中文名称 | 吡啶-N-氧化物 |
| 英文名称 | Pyridine-N-oxide |
| CAS号 | 694-59-7 |
| 分子式 | C5H5NO |
| 分子量 | 95.1 |
| EINECS号 | 211-774-6 |
| 熔点 | 62-67 °C(lit.) |
| 沸点 | 270 °C(lit.) |
| 密度 | 1.1418 (rough estimate) |
| 折射率 | 1.5939 (estimate) |
| 闪点 | 143 °C |
| 形态 | 结晶固体、晶体和/或块 |
| 酸度系数(pKa) | 0.79(at 24℃) |
| 颜色 | 白色至褐色 |
| 水溶解性 | soluble |
| 敏感性 | Hygroscopic |
| 默克索引编号 | 14,7972 |
| BRN | 105257 |
| 危险品标志 | Xi,Xn |
| 危险类别码 | 36/37/38-22-40-20/21/22 |
| 安全说明 | 26-24/25-37/39-36/37/39-22 |
| WGK Germany | 3 |
| RTECS号 | UT6410000 |
| TSCA | Yes |
| 海关编码 | 29333999 |
吡啶N-氧化物是一类稳定的有机化合物,可作为起始原料合成吡啶衍生物。以储量丰富、容易获得的烯烃为烷基化试剂,实现吡啶N-氧化物到邻位烷基取代吡啶的转化,这种思路十分有吸引力。然而,这类报道仅有少数几例,而且只适用于缺电子烯烃。例如,全氟丙烯与吡啶N-氧化物通过1,3-偶极环加成和碳酰氟消除反应得到四氟乙基取代的吡啶(图1a,J. Org. Chem. 1968, 33, 3343–3344;Mendeleev Commun. 2006, 16, 161–163)。尽管吡啶N-氧化物中含有极性N–O键,但对于环加成反应来说,它们的1,3-偶极子活性较低,其原因可能是反应中两个底物的芳香性同时被破坏。解决这个问题的办法之一是以光催化简单烯烃生成的自由基物种作为吡啶N-氧化物的烷基化组分。因为这类阳离子自由基具有足够的亲电性,可与吡啶N-氧化物偶联生成自由基中间体,再经过分子内邻位加成和羰基化合物消除之后,便可得到邻位取代的吡啶产物。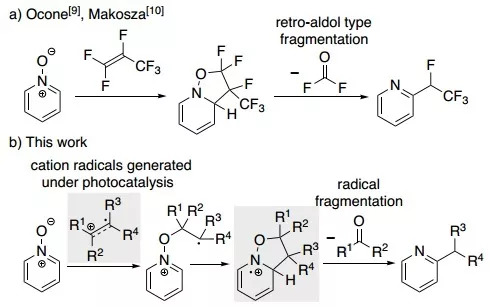
图1. 吡啶N-氧化物转化为邻位烷基取代吡啶
(来源:Angew. Chem. Int. Ed.)
1.用过氧邻苯二甲酸氧化吡啶制取。
2.在装有搅拌器、温度计和滴液漏斗的1升三颈瓶中,放入110克(1.39摩尔)吡啶,在搅拌及保持85℃的条件下,加入250的毫升(285克,1.50摩尔)40%物过氧乙酸(用10%或20%过氧乙酸亦可)。需事50一60分钟加完。继续搅拌直至混合物温度降至40用碘化钾溶液检查乙酸证明不含过氧化物时,在水汽浴上及水泵减压下蒸发乙酸溶液。残余物(180一190克)在》1mm压力下蒸馏,收集固体蒸出物。真空泵必需用干冰冷阱保护(冷 阱中可能收集吡啶氧化物乙酸盐在低压下离解产生的约60毫升乙酸)。用油浴加热,不要让温度升到130℃以上。得103-110克(78-83%)无色固体。
-
CAS号:53937-02-3
4-苄氧基-2(1H)-吡啶酮 -
CAS号:6935-27-9
2-苯甲基氨基吡啶 -
CAS号:29082-91-5
4-甲氧基吡啶-2-甲酸 -
CAS号:3811-73-2
吡啶硫酮钠 -
CAS号:14305-17-0
2-溴吡啶-N-氧化物 -
CAS号:25700-11-2
2-(1-吡唑基)吡啶 -
CAS号:626-61-9
4-氯吡啶 -
CAS号:879088-41-2
4-氯-3-(吡啶-2-基)苯胺 -
CAS号:19235-89-3
4-氯-2-氰基吡啶 -
CAS号:1122-61-8
4-硝基吡啶 -
CAS号:2859-68-9
2-吡啶丙醇 -
CAS号:19235-88-2
2-氰-4-硝基吡啶 -
CAS号:1122-96-9
4-甲氧基吡啶-N-氧化物 -
CAS号:13509-19-8
4-硝基-2-吡啶甲酸 -
CAS号:504-24-5
4-氨基吡啶
-
CAS号:628-13-7
吡啶盐酸盐 -
CAS号:2893-33-6
2,6-吡啶二甲腈 -
CAS号:18820-82-1
吡啶氢溴酸盐 -
CAS号:1003-67-4
4-甲基吡啶氧化物 -
CAS号:65938-88-7
吡啶-4-磺酰胺 -
CAS号:34981-10-7
2,3,5,6-四氨基吡啶三盐酸盐 -
CAS号:3811-73-2
吡啶硫酮钠 -
CAS号:464-05-1
三氟乙酸吡啶 -
CAS号:5346-38-3
吡啶-2-硫代酰胺 -
CAS号:63636-89-5
吡啶-2-磺酰胺 -
CAS号:4591-55-3
3,5-吡啶二甲酸甲酯 -
CAS号:29800-89-3
吡啶-4-乙酸甲酯 -
CAS号:873-69-8
2-吡啶甲醛肟 -
CAS号:878376-35-3
吡啶-2-磺酰氟 -
CAS号:26412-87-3
三氧化硫吡啶 -
CAS号:4664-08-8
吡啶-3,4-二羧酸酐 -
CAS号:13602-12-5
异烟酸-N-氧化物


