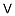
| 中文名称 | Vanadium |
| 英文名称 | Vanadium |
| CAS号 | 7440-62-2 |
| 分子式 | V |
| 分子量 | 0 |
| EINECS号 | 231-171-1 |
| 熔点 | 1890 °C(lit.) |
| 沸点 | 3380 °C(lit.) |
| 密度 | 6.11 g/mL at 25 °C(lit.) |
| 蒸气压 | 8 mm Hg ( 20 °C) |
| 溶解度 | 可溶于水中 |
| 形态 | 碎屑状物质 |
| 颜色 | 银灰 |
| 比重 | 6.11 |
| 电阻率 (resistivity) | 24.8-26.0 μΩ-cm, 20°C |
| 水溶解性 | insoluble H2O; reacts with hot H2SO4, HF, HNO3, aqua regia [MER06] |
| 默克索引编号 | 13,9984 |
| 暴露限值 | OSHA: Ceiling 0.5 mg/m3; Ceiling 0.1 mg/m3NIOSH: TWA 1 mg/m3; STEL 3 mg/m3; Ceiling 0.05 mg/m3 |
| 稳定性 | 稳定的。与强酸、强氧化剂不相容。 |
| 危险品标志 | Xi,T+,N,Xn |
| 危险类别码 | 36/38-36/37/38-34-26-22-50-20 |
| 安全说明 | 26-36-45-7-36/37/39-28-61 |
| 危险品运输编号 | UN 3289 6.1/PG 2 |
| WGK Germany | 3 |
| RTECS号 | YW1355000 |
| TSCA | Yes |
| 海关编码 | 8112 92 91 |
| 危险等级 | 4.1 |
| 包装类别 | II |
| 毒害物质数据 | 7440-62-2(Hazardous Substances Data) |
| 毒性 | LD50 orally in Rabbit: > 2000 mg/kg |
钒:元素符号 V,银灰色金属,在元素周期表中属VB族,原子序数23,原子量50.9414。钒属于中等活泼的金属,化合价+2、+3、+4和+5。其中以5价态为最稳定,其次是4价态,五价钒的化合物具有氧化性能,低价钒则具有还原性。钒的价态越低还原性越强。电离能为6.74电子伏特,具有耐盐酸和硫酸的本领,并且在耐气、耐盐、耐水腐蚀的性能要比大多数不锈钢好。钒空气中不被氧化,可溶于氢氟酸、硝酸和王水。
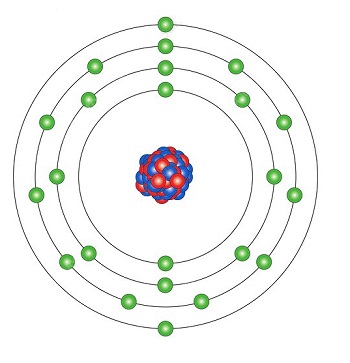
钒是浅灰色或银白色,易延展的固体,光泽粉末或熔融硬块。不溶于水;耐腐蚀,但可溶于硝酸,氢氟酸和浓硫酸;受碱侵蚀,形成水溶性钒酸盐。充当金属或非金属,并形成各种复杂的化合物。钒的性质和钽以及铌相似,英国化学家罗斯科研究了它的性质,确定它与钽和铌相似,这为它们三个在元素周期表中共建一个分族建立了基础。

钒于1801年由墨西哥矿物学家Manuel del Rio在墨西哥伊达尔戈的铅矿石中发现。他将其命名为erythronium,因为在用酸加热时其盐呈红色。但是,当时del del Rio的发现被错误地认为是不纯铬的一种形式。瑞典化学家塞夫斯特伦(Sefstrom)在1830年重新发现了这种元素,在瑞典塔贝格(Taberg)的铁矿石中发现了一种未知金属。他以斯堪的纳维亚女神Vanadis的名字命名为钒。 1830年下半年,Wohler确定del Rio的erythronium和Sefstrom的钒是同一元素。 Roscoe于1867年首次通过用氢气还原氯化钒VCl2,以银白色粉末形式首次制备了不纯形式的钒金属。亨特(Hunter)和琼斯(Jones)在1923年通过在钢弹中用钠热还原三氯化钒与钠来制备纯度为99.5%的金属,为灰色细粉。
钒的主要用途是作为一种合金金属来制造坚固且耐腐蚀的钢材,非常适合诸如核反应堆之类的结构。它不像普通不锈钢那样吸收中子或因热和应力而“拉伸”,因此使钒成为建造核反应堆的理想之选。钒的某些化合物,特别是氧化物,在化学工业中用作催化剂,以加速有机化学反应。反应。黄棕色五氧化二钒(V2O5)用作催化剂,以促进通过接触法生产硫酸。五氧化二钒还用作照相显影剂,以使纺织品染色以及用于人造橡胶的生产。当与玻璃结合使用时,它可以作为过滤器以抵抗阳光中的紫外线。钒没有纯的单质状态存在。在磷酸盐岩和一些铁矿石中可以发现少量钒。它的大部分是从两种矿物中回收的:钒铅矿(一种铅和氯加上一些氧化钒的化合物)和卡诺石(一种含有铀,钾和钒氧化物的矿物)。由于钒具有四种氧化态,并且既可以作为金属也可以作为非金属,因此可以与55种以上的化学元素化学结合。钒的主要矿石是爱达荷州发现的轮锰铁矿,镁橄榄石,钒铁矿和卡诺石。蒙大拿州,阿肯色州和亚利桑那州以及墨西哥和秘鲁,也是磷酸盐矿生产的副产品。钒属于非必需但有益于植物生长的有益元素类别。它是对绿藻非常有用的营养素,但尚未确定高等植物生长所需的确切钒量。 钒在固氮作用下可以通过固氮菌和根瘤菌等微生物替代钼。在芦笋,大米,生菜,大麦和玉米中,钒引起的生长增加。还已经推测钒可以在生物氧化还原反应中起作用。 在没有钼的情况下,钒刺激鱼腥藻的生长和固氮酶活性。低浓度的钒有利于微生物和高等植物的最佳生长。通常,植物中钒的浓度约为1 ppm。
世界上钒资源超过6300万吨。钒存在于磷酸盐岩,钛铁矿磁铁矿,铀铁质砂岩和粉砂岩矿床中,其中钒含量不到基质岩的2%。铝土矿和石炭系材料中也存在大量铝土,石油,原油,油页岩和le石(19)。 钒通常在提取其他化合物(例如铁,钛,磷酸盐或石油)过程中作为副产物或副产物回收。它从卡诺石,磷矿床,钛磁铁矿和钒粘土中提取。在萃取的初始阶段,称为盐焙烧的过程会产生氧化物精矿。将铁钒酸盐生产过程中形成的矿石,石油残留物,碘化物热分解产物和矿渣压碎,干燥,细磨,与钠盐混合并烘烤。含有偏钒酸钠的热矿石以红色饼的形式沉淀,然后与硫酸混合,沉淀出的沉淀物经干燥形成五氧化二钒。然后可以进一步加工五氧化二钒以形成所需的钒化合物。纯钒很难获得,因为它容易被其他元素污染。提取纯钒的方法包括碘化精制,熔融盐中的电解精制和电传输。最高纯度的钒已通过电传输技术纯化。高纯度延性钒可通过用镁或镁-钠混合物还原氯化钒来获得。现在,通过在压力容器中还原V2O5的钙可生产许多钒金属。
钒粉,灰尘和大多数氧化物化合物在暴露于热和空气中时会爆炸。 吸入也有毒。 氯化钒化合物对皮肤有强刺激性,食入时有毒。 它的许多化合物必须存储在干燥,无氧的气氛中或惰性气体容器中。 处理钒以及大多数其他过渡元素时,应穿戴防护服和护目镜。储存于阴凉、通风的库房。远离火种、热源。应与氧化剂、酸类、食用化学品分开存放,切忌混储。配备相应品种和数量的消防器材。储区应备有合适的材料收容泄漏物。金属钒的毒性很低。钒化合物(钒盐)对人和动物具有毒性,其毒性随化合物的原子价增加和溶解度的增大而增加,如五氧化二钒为高毒,可引起呼吸系统、神经系统、胃肠和皮肤的改变。钒电池是目前发展势头强劲的优秀绿色环保蓄电池之一(它的制造、使用及废弃过程均不产生有害物质),它具有特殊的电池结构,可深度大电流密度放电;充电迅速;比能量高;价格低廉;应用领域十分广阔:如可作为大厦、机场、程控交换站备用电源;可作为太阳能等清洁发电系统的配套储能装置;为潜艇、远洋轮船提供电力以及用于电网调峰等。钒电池成本与铅酸电池相近,它还可制备兆瓦级电池组,大功率长时间提供电能,因此钒电池在大规模储能领域具有锂离子电池、镍氢电池不可比拟的性价比优势。钒电池生产工艺简单,价格经济,电性能优异,与制造复杂、价格昂贵的燃料电池相比,无论是在大规模储能还是电动汽车动力电源的应用前景方面,都更具竞争实力。钒是人体必需的微量元素在人体内含量大约为25mg,在体液pH4~8条件下 钒的主要形式为VO-3,即亚钒酸离子(metavandate);另一为+5价氧化形式VO4- 3即正钒酸离子(orthovanadate)。由于生物效应相似,一般钒酸盐(Va)统指这两种+5价氧化离子。VO-3经离子转运系统或自由进入细胞,在胞内被还原型谷胱甘肽还原成VO2+(+4价氧化态),即氧钒根离子(vanadyl)。由于磷酸和Mg2+离子在细胞内广泛存在VO-3与磷酸结构相似,VO2+与Mg2+大小相当(离子半径分别为160pm和165pm),因而二者就有可能通过与磷酸和Mg2+竞争结合配体干扰细胞的生化反应过程。例如,抑制ATP磷酸水解酶、核糖核酶磷酸果糖激酶、磷酸甘油醛激酶、6-磷酸葡萄糖酶、磷酸酪氨酸蛋白激酶。所以,钒进入细胞后具有广泛的生物学效应。钒化合物又具有合成相对容易、价格较低廉的优势,因此研究钒化合物的降压机制有利于对钒的开发和利用。钒的性质和钽以及铌相似,英国化学家罗斯科研究了它的性质,确定它与钽和铌相似,这为它们三个在元素周期表中共建一个分族建立了基础。钒属于中等活泼的金属,化合价+2、+3、+4和+5。其中以5价态为最稳定,其次是4价态,五价钒的化合物具有氧化性能,低价钒则具有还原性。钒的价态越低还原性越强。电离能为6.74电子伏特,具有耐盐酸和硫酸的本领,并且在耐气、耐盐、耐水腐蚀的性能要比大多数不锈钢好。钒空气中不被氧化,可溶于氢氟酸、硝酸和王水。纯的金属钒一般是用钾在高压下将五氧化二钒还原而得到的。大多数钒是其它矿物加工时的副产品。工业上也可以以铝,焦炭还原五氧化二钒生产纯钒。
焦炭还原五氧化二钒生产纯钒是将V2O5粉与高纯碳粉混合均匀,加10%樟脑乙醚溶液或酒精,压块后放入真空碳阻炉或感应炉内。炉内真空压力到6.66×10-1Pa后,升温至1573K,保温2h。冷却后将反应产物破碎。根据第一次还原产物的组分再配入适量碳化钒或氧化钒进行二次还原。二次还原炉内的真空压力为2.66×10-2Pa,温度控制在1973~2023K之间,并保温一段时间。真空碳还原法所得金属钒的成分(质量分数m/%)为:钒99.5,氧0.05,氮0.01,碳0.1。钒收率可达98%~99%。[7] 铝热还原法是将五氧化二钒和纯铝放在反应弹进行反应,生成钒铝合金。钒合金在2063K的高温和真空中脱铝,可制得含钒94%~97%的粗金属钒。皮肤接触:脱去污染的衣着,用肥皂水及清水彻底冲洗。眼睛接触:立即翻开上下眼睑,用流动清水冲洗15分钟。就医。吸入:脱离现场至空气新鲜处,用水漱洗鼻咽部的粉尘。就医。食入:误服者就医。对症治疗。在钢中加入百分之几的钒,就能使钢的弹性、强度大增 ,抗磨损和抗爆裂性极好,既耐高温又抗奇寒,难怪在汽车、航空、铁路、电子技术、国防工业等部门,到处可见到钒的踪迹。此外,钒的氧化物已成为化学工业中最佳催化剂之一,有“化学面包”之称。主要用于制造高速切削钢及其他合金钢和催化剂。把钒掺进钢里,可以制成钒钢。钒钢比普通钢结构更紧密,韧性、弹性与机械强度更高。钒钢制的穿甲弹,能够射穿40厘米厚的钢板。但是,在钢铁工业上,并不是把纯的金属钒加到钢铁中制成钒钢,而是直接采用含钒的铁矿炼成钒钢。
钒具有众多优异的物理性能和化学性能,因而钒的用途十分广泛,有金属“维生素”之称。最初的钒大多应用于钢铁,通过细化钢的组织和晶粒,提高晶粒粗化温度,从而起到增加钢的强度、韧性和耐磨性。后来,人们逐渐又发现了钒在钛合金中的优异改良作用,并应用到航空航天领域,从而使得航空航天工业取得了突破性的进展。随着科学技术水平的飞跃发展,人类对新材料的要求日益提高。钒在非钢铁领域的应用越来越广泛,其范围涵盖了航空航天、化学、电池、颜料、玻璃、光学、医药等众多领域。钒是一种银灰色的金属。熔点1890±10℃,属于高熔点稀有金属之列。它的沸点3380℃,纯钒质坚硬,无磁性,具有延展性,但是若含有少量的杂质,尤其是氮,氧,氢等,能显著降低其可塑性。钒在天然水中的浓度很低,一般河水中为0.01~20ppb,平均为1ppb。海水含钒量为0.9~2.5ppb。尽管水体中可溶性的钒含量很低,但是水中悬浮物含钒量是很高的。悬浮物的沉积导致水中钒向底质迁移,并使水体得到净化。土壤中的钒主要以VO3-阴离子状态存在。土壤的氧化性越高、碱性越大,钒越易形成VO3-离子。当土壤的酸度增大时,VO3-离子易转变成多钒酸根复合阴离子。它们都容易被粘土和土壤胶体及腐殖质固定而失去活性,钒在土壤中的迁移性较弱。
1.主要矿物有钒酸钾铀矿、铅钒矿等。用钙还原五氧化二钒或用镁还原三氯化钒制得。
2.首先在碳存在下,将V2O5于约750℃下进行氯化,生成四氯化钒VCl4。由于生成VCl4的同时还生成三氯一氧化钒VCl3O,故需将VCl3O在碳存在下,于约750℃进一步氯化,使生成VCl4。然后在干燥的二氧化碳气流中,使VCl4在其沸点(148.5℃)温度下回流,再加热使分解为VCl3。将制得的VCl3进一步蒸馏得到纯度为99.8%的VCl3。最后将这种VCl3在约850℃温度下用镁还原,就可制得质量很好的金属钒。
-
CAS号:68553-60-6
环烷酸氧化钒 -
CAS号:123334-20-3
硫酸氧钒(IV) 水合物 -
CAS号:13476-99-8
乙酰丙酮钒 -
CAS号:3153-26-2
乙酰丙酮氧钒 -
CAS号:1314-34-7
三氧化二钒(III) -
CAS号:14767-37-4
二(1-苯基-1,3-丁二酮)氧代钒(Ⅳ) -
CAS号:12439-96-2
水合硫酸氧钒 -
CAS号:27860-55-5
八乙基卟吩氧钒(IV) -
CAS号:24646-85-3
氮化钒 -
CAS号:13709-31-4
三氟代氧化钒 -
CAS号:12036-21-4
四氧化二钒 -
CAS号:7727-18-6
三氯氧钒 -
CAS号:7803-55-6
偏钒酸铵 -
CAS号:68553-60-6
环烷酸氧化钒 -
CAS号:123334-20-3
硫酸氧钒(IV) 水合物 -
CAS号:13476-99-8
乙酰丙酮钒 -
CAS号:3153-26-2
乙酰丙酮氧钒 -
CAS号:1314-34-7
三氧化二钒(III) -
CAS号:14767-37-4
二(1-苯基-1,3-丁二酮)氧代钒(Ⅳ) -
CAS号:12439-96-2
水合硫酸氧钒 -
CAS号:27860-55-5
八乙基卟吩氧钒(IV) -
CAS号:24646-85-3
氮化钒 -
CAS号:13709-31-4
三氟代氧化钒 -
CAS号:12036-21-4
四氧化二钒 -
CAS号:7727-18-6
三氯氧钒 -
CAS号:7803-55-6
偏钒酸铵


